近日,杨巍副教授团队在Advanced Science(IF5y = 16.3)和Journal of Nanobiotechnology(IF5y = 11.4)连续发表两项重要研究成果,分别揭示了脱氧雪腐镰刀菌烯醇(DON)诱发厌食及厌恶样情绪障碍的神经机制,以及细胞外囊泡负载二氧化铈纳米颗粒缓解DON致肝损伤的分子机制。研究成果由杨巍老师作为通讯作者指导完成,博士研究生杨柳楠(2021级)和孟子桐(2020级)分别为两篇论文的第一作者,华中科技大学同济医学院公共卫生学院为第一完成单位。
论文一:
Regulation of PVT-CeA Circuit in Deoxynivalenol-Induced Anorexia and Aversive-Like Emotions
(Advanced Science, 2025)
脱氧雪腐镰刀菌烯醇(DON,又称呕吐毒素),是粮食储存和加工过程中由镰刀菌属产生的一种高稳定性毒素,由于其耐高温、耐酸碱的特性,常规食品加工脱毒工艺难以彻底清除,使其成为全球范围内广泛存在的食源性污染物。当DON进入体内后,会引发严重的厌食和厌恶样情绪反应,但此前关于其具体作用脑区及神经环路机制的研究仍不够深入。
为破解这一难题,杨巍老师团队综合运用光遗传学、化学遗传学及全细胞膜片钳等技术发现DON会特异性干扰大脑中央杏仁核 (CeA) 的GABA能神经元(CeAGABA)功能,并破坏丘脑室旁核 (PVT) →CeA神经环路的信息传递,从而诱发厌食及厌恶样情绪。更重要的是,通过进一步的脑组织转录组学测序发现,经口灌胃DON后,CeA脑区的钙离子通道SCN10A表达水平显著增高,而通过脑内套管施用SCN10A拮抗剂(A-803467)后,可有效改善小鼠的进食行为并促进体重恢复。这项研究不仅揭示了DON致厌食及厌恶样情绪的关键神经机制,还发现了SCN10A这一潜在干预靶点,为未来开发DON减毒策略提供了重要理论依据(图一)。

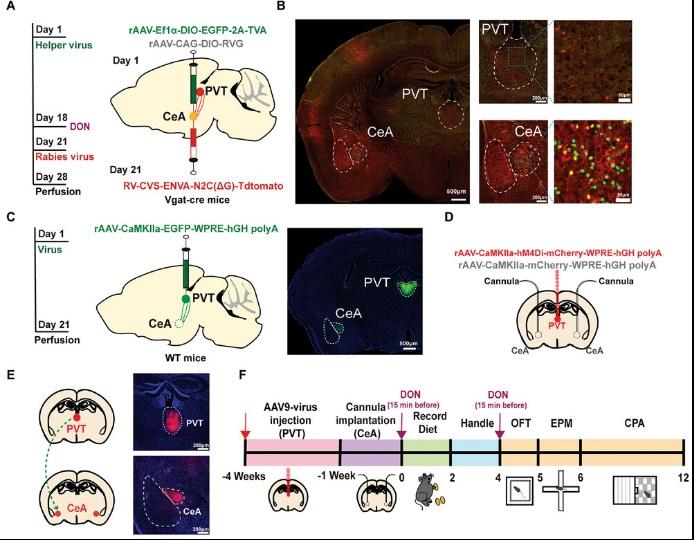
图一:DON干扰脑区神经元投射和离子通道致厌食及厌恶样情绪产生的机制示意图。
论文二:
Protective effects of bone marrow mesenchymal stem cell-derived exosomes
loaded cerium dioxide nanoparticle against deoxynivalenol-induced liver damage
(Journal of Nanobiotechnology, 2025)
DON进入体内后,肝脏作为首要代谢器官承担着重要解毒功能。然而,DON分子中的羟基基团会引发强烈氧化应激,导致肝细胞损伤。传统抗氧化物质(如维生素C、白藜芦醇、姜黄素等)虽然具有一定的缓解作用,但普遍存在靶向性不足、代谢过快等缺陷,难以实现长效肝脏保护作用。
骨髓间充质干细胞外泌体(BMSC-exos)是一类粒径范围在50-150 nm的细胞外囊泡,其表面富含CD9和CD63等特征性跨膜蛋白,独特的膜脂质组成赋予其优异的生物相容性和细胞靶向性,能够有效触发"Eat me"信号并促进细胞摄取,展现出理想的药物递送特性。与此同时,二氧化铈纳米颗粒 (18-25 nm) 因其镧系金属特性,作为新型抗氧化材料,已在干眼症和抗肿瘤治疗等领域展现出临床应用价值。
结合上述物质的理化特性,杨巍老师团队利用膜挤压法(Avantimini extruder)将二氧化铈纳米颗粒封装入BMSC-exos,构建BMSC-exos@CeO2纳米复合物,并通过ICP-MS检测发现该复合物在肝脏的滞留时间可长达72 h以上,显著优于传统抗氧化剂。进一步通过整合氧化脂质组学、蛋白组学及代谢组学等多组学分析,团队发现BMSC-exos@CeO2能够通过调控细胞内稳态调控元件AMPK,有效抑制JAK1/STAT3脂质过氧化信号通路,从而阻断氧化应激的级联反应,显著减轻DON诱导的肝细胞损伤(图二)。这项研究不仅深入揭示了DON致肝损伤的分子机制,更重要的是开发了一种基于外泌体-纳米协同作用的新型解毒策略,为食品安全防护和靶向解毒治疗提供了新的的解决方案,具有重要的科学意义和临床应用前景。
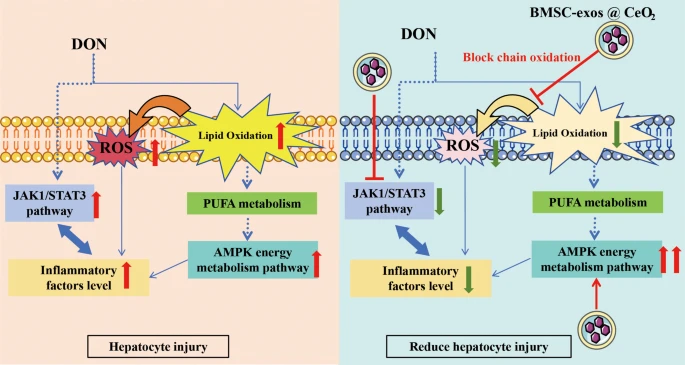

图二:BMSC-exos@CeO2复合物通过AMPK/JAK1/STAT3信号通路缓解DON致肝损伤的机制示意图。

